糖尿病等慢性疾病的综合管理
–必需金属及有毒金属与2型糖尿病关系篇
成 长
前言:
2型糖尿病(T2DM)影响着全世界数亿人。据世界卫生组织2016年估计,中国约10%的人口,即超过一亿人(~1.1亿)是2型糖尿病病人[1]。据美国疾控中心(CDC)2017年报告,美国的糖尿病发病率与中国相近,也在~10%,~3千万糖尿病病人;糖尿病前期病人~占总人口25%,~8千4百万。美国目前有超过一亿人是糖尿病糖或尿病前期病人。到2050年,糖尿病总人口将翻3倍,占美国总人口的1/3。如果不加干预,糖尿病前期病人一般5年内发展为临床糖尿病[2]。
糖尿病是一主要流行病,给全人类带来巨大健康,经济负担。糖尿病的综合管理已经刻不容缓。糖尿病的综合管理必须是一个政府,企业,民间,以及医药界与消费者的共同合作,团结共赢的合作。否则,糖尿病将会给个人,家庭,社会,及政府带來沉重的,不可持续的健康,经济负担。
低碳/生酮饮食用于糖尿病管理在过去几年中在世界范围内,在大众及部分医务人员中引起了越来越广泛的关注。关于低碳/生酮饮食用于糖尿病治疗的临床研究越来越多,是治疗糖尿病的第一步,也是非常重要的一步。低碳/生酮饮食者用于糖尿病的治疗肯定无疑地是一个里程碑式的进展,但认为低碳/生酮饮食是“一刀切”的能解决糖尿病全部问题的灵丹妙药,可能会产生失望及误导。与大部分慢性疾病一样,糖尿病也是一个多因素疾病,是各种外源性糖尿病致病剂(diabetogen),如饮食中糖过多,金属,非金属毒素过量等,加上内源性因素,如睡眠运动营养等不足,导致人体一系列的代谢紊乱,最后致病。糖尿病不是一个单因素疾病,管理手段也不应该是单一的。本文将试图以多篇文章的形式,系统综合分析各种因素,最后并提出一个综合性的预防,治疗,管理方案。
环境污染(金属及非金属化学品)与2型糖尿病关系
天然存在的金属无机元素,在生命组织中的含量很少,但对生命的重要过程至关重要[3]。一些金属(例如镁)被称为常量金属(相对于稀有元素),在人体组织中含量很高,因此它们也被称为常量营养素(macro nutrients)[4]。常量营养素是指日常饮食中每种至少需要100 mg的营养素[5]。相反,某些金属例如体内所需的铜(Cu),锌(Zn),铁(Fe)和锰(Mn),铬(Cr)等非常少量,少于百万分之100(ppm),因此称为微量元素或微量营养素[6]。镁,锌,铬,铁,錳,铜等各种金属被认为对正常人体健康至关重要[3,7]。金属参与各种生理过程,例如许多蛋白质的修复基团,水平衡,多种酶的辅因子等[8]。几种金属作为金属蛋白酶/金属酶作为蛋白质/酶的一部分[9]。这类不含金属的修复基团的蛋白质无法执行其生理功能[10]。调节身体中各种金属含量是其正常功能的前提[11]。金属使肌肉收缩或放松,并通过神经传递冲动。大多数金属以可溶性盐形式存在,可调节生物流体的组成。微量元素的适当代谢功能取决于它们在各种身体组织中的正常水平[12]。
但是工农业革命及快速经济发展,尤其是过去三四十年的中国,也带来了环境污染,包括各种有毒金属和化学物质。这些环境毒素污染了我们的食物,水,空气以及我们日常生活中接触的所有事物。它们是导致当今慢性病猖獗的重要原因。对于每个人,尤其是医疗保健专业人员,识别,测试和采取措施以预防和抵抗,驱除或减少它们的影响至关重要。
必需金属及其生理作用:
累积的证据表明这些金属对于维持人类正常生理至关重要。这些金属的失衡与糖尿病及糖尿病并发症发生密切相关。这些金属的失衡不纠正,糖尿病及其他慢病难以得到根本上的预防,治疗。
铁(Fe):糖尿病患者和其他慢性病患者中铁蛋白往往较高,提示铁过量。血清铁蛋白水平可能成为糖尿病的替代标志物,以预测糖尿病的发生。
铁是血红蛋白和肌红蛋白合成所必需的重要金属。铁与锌,維生素C一样,也是弹性蛋白和胶原蛋白的合成中所必須的[13]。在血液中,一小部分血清铁被糖蛋白(称为转铁蛋白)转运到细胞中[14]。铁蛋白是人体组织内储存游离铁的方式。铁蛋白在新诊断的糖尿病患者中铁的含量增加[15,16]。与非糖尿病患者相比,糖尿病患者的铁蛋白水平更高。最近,有报告显示血清铁蛋白越高,组织中的铁沉积越多,随糖尿病持续时间呈线性增加[17]。血清铁蛋白升高被认为是铁超负荷的指标,严重时可导致血色病[18]。多项研究表明血色病与2型糖尿病之间存在关联[19–21]。高铁水平是细胞内氧化压力升高的主要原因,会氧化各种生物分子,例如核酸,蛋白质和脂质,这可能通过减少胰腺β细胞的胰岛素分泌以及胰岛素抵抗的增加而促进T2D的发展[22–26]。研究显示血清铁蛋白水平与在糖尿病前期,胰岛素抵抗之间存在很强的关系[27,28]。除葡萄糖升高外,血清铁蛋白水平可能成为糖尿病的替代标志物,以预测疾病的发作[29,30]。
镁(Mg):糖尿病,妊娠糖尿病人镁偏低。镁在胰岛素抵抗,糖尿病发生发展,预防治疗中占有重要地位。
镁是最丰富的常量营养素(macro nutrient)之一,对于维持适当的健康至关重要。300多种酶的活性需要镁,这些酶在人体中具有多种重要的生理功能[31,32]。含镁的酶参与葡萄糖的稳态,神经传递,DNA和RNA的产生[33]。镁在调节胰岛β细胞的胰岛素分泌中起重要作用,并改善胰岛素受体的胰岛素结合[34,35]。已证明镁缺乏可能导致胰岛素介导的葡萄糖摄取减少[31,36]。另一方面,补充镁可预防胰岛素抵抗,并减少糖尿病的发展[37]。一些研究报道,相对于健康对照者,糖尿病患者血清中的镁含量较低,而尿中镁的排泄量增加[36]。研究显示口服镁补充剂可降低血糖,血压和甘油三酸酯[37]。镁缺乏是导致糖尿病发展和恶化的主要因素。低镁似乎是胰岛素抵抗的直接原因之一[38]。今年(2019)的一項荷兰的大型PREVEND研究对5747名最初无糖尿病的受试者进行了研究,隨訪了11年,血浆镁水平低与女性患糖尿病的风险更高独立相关[39]。最近的一项随访了29年涉及14353名受试者的研究显示,美国成年人的血清镁浓度极低与全因死亡率增加的风险显着相关[40]。长期较低的镁明显促进胰岛素抵抗,持续补充镁明显提高血清和细胞内镁浓度。补充镁似乎可以改善胰岛素介导的细胞葡萄糖摄取, 改善对胰岛素的抵抗力[41–44]。对13,525名日本人进行的一项为期10年的研究表明,高镁摄入量可降低糖尿病风险[45]。 在对3个队列,总计200,000多人进行了长达28年的综合分析后,研究人员表明,较高的镁摄入量可降低糖尿病的患病风险,尤其是与低碳饮食結合时[46]。在糖尿病患者中,高镁摄入和高血清镁可降低冠心病的风险[47]。 在动物研究中,镁似乎不仅会降低胰岛素抵抗,还会增加胰岛素受体和葡萄糖转运蛋白,这些都是糖尿病的标志[48–50]。在许多糖尿病患者中,存在低镁导致胰岛素抵抗和胰岛素抵抗导致镁缺乏的恶性循环[34,51]。一项双盲随机试验显示,在非糖尿病人群中,镁被证明能够根据需要改善β细胞分泌胰岛素的能力[52]。低镁水平可抑制非糖尿病患者的胰岛素分泌[53]。镁水平低的糖尿病患者往往发展更快,并发症更多[54]。
与正常孕妇或非孕妇相比,妊娠糖尿病妇女还显示出低镁[55]。镁和维生素E的补充可显着改善妊娠糖尿病妇女的血糖控制和血脂水平[56]。
锰(Mn)
锰在多种酶(包括与骨髓产生有关的酶以及碳水化合物,蛋白质和脂肪的代谢)中充当辅助因子[57]。这对于正确利用胆碱,硫胺素,生物素,维生素C和维生素E是必不可少的。锰作为酶的辅助因子也参与线粒体糖蛋白的合成[58]。由于缺乏锰,这些酶的活性受损,导致软骨生成异常[59]。锰也是丙酮酸羧化酶的辅因子,其在通过糖异生作用将各种非碳水化合物转化成葡萄糖用于随后的使用中起作用。简而言之,锰也是正常胰岛素合成,其分泌以及代谢改变涉及糖尿病发展所必需的[3]。Forte等一项研究发现2型糖尿病患者锰缺乏[60]。
铜(Cu)
铜是另一种必需的矿物质,它具有多种生物学功能。超氧化物歧化酶(SOD)的催化活性是必需的,它参与保护细胞免受超氧化物自由基的侵害[61]。铜的不平衡与正常的高密度脂蛋白(HDL)和低密度脂蛋白(LDL)平衡的破坏有关[62]。铜还激活线粒体电子传输链中涉及的细胞色素氧化酶[63]。在缺铜的情况下,细胞色素氧化酶会降低其活性,这可能导致代谢活性组织(如胰腺腺泡细胞,肝细胞等)中的线粒体变形[64,65]。已有的研究表明,铜缺乏是导致心血管疾病发展的原因之一[66]。其他报道表明,铜还有助于预防关节炎相关的炎症和癫痫病[67]。铜水平的紊乱与糖尿病的代谢途径及其并发症相关的异常有关[3,68]。铜以及锌金属起着保护人体组织氧化损伤的作用[69,70]。
锌(Zn)
锌是一种必需的微量元素,参与多种生化途径,例如转录,翻译,细胞分裂和凋亡[71]。 300多种酶需要锌才能发挥催化活性。从催化位点除去锌会导致各种酶的活性丧失[72]。约70%的锌与白蛋白结合,白蛋白的任何病理改变都会影响血清中的锌水平[73]。锌吸收不良会导致各种类型的疾病,包括皮肤,胃肠道,神经和免疫异常[74]。
铬(Cr)
铬的生物活性取决于其价态及其形成的化学络合物[12,75]。铬的三价形式具有很高的生物活性,是细胞最佳摄取葡萄糖所必需的[75,76]。铬通过上调肌肉细胞中的葡萄糖转运蛋白(GLUT4)的转运来刺激胰岛素信号传导途径和代谢,从而调节胰岛素和血糖水平[77]。铬缺乏症会导致血糖水平升高,如果长期坚持下去,可能导致糖尿病的发展[78]。一些报告表明,铬补充剂可降低糖尿病患者的血糖水平[79]。长时间的高血糖会增加铬的尿排泄[3,60]。
有毒金属与健康,慢病尤其是糖尿病的关系:
铅,砷,锌,镉,汞和镍等超标时,都是强力的氧化剂,可以促进糖尿病等慢性病甚至癌症的发生[80]。
有毒金属铅(Pb),镍(Ni),镉(Cd)和砷(As)等进入体内后,沉积在组织中并且不可降解。因此,这些金属通常长时间保留在组织中,带来的问题通常难以消除。人体组织可以忍受一定水平的金属。超过此阈值限制,组织会由于金属毒性而受到损坏。一些有毒金属,包括镍,砷等被证明是致癌物[81–83]。
铅(Pb)
据报道,糖尿病人的生物样品(即血浆和尿液)中的某些有毒金属(包括铅)的浓度高于非糖尿病人[84]。铅对人体大多数器官有害,并干扰新陈代谢和细胞功能[85]。研究显示,与年龄有关的疾病中血铅水平与肾功能不全之间存在线性关系。这可能是由于经常暴露于环境铅有关[86]。研究表明,接触铅会严重影响抗氧化途径[83]。现有证据表明,金属诱导的毒性可能导致活体组织中抗氧化机制的紊乱。结果产生了活性氧(ROS)。这种抗氧化剂的不平衡可能导致蛋白质,核酸和脂质过氧化降解。 ROS对细胞成分的氧化攻击与包括糖尿病在内的几种人类疾病的发病机制有关[87,88]。事实上绝大部分(如果不是所有)慢性病都与氧化压力升高相关。
镉(Cd)
镉是一种重金属,广泛存在于空气,水和土壤等环境中。水中镉的增加被植物,动物和人类吸收[84]。经常接触镉会导致其在肾脏中的过量积累,从而导致肾脏损害和肾病[87]。此外,高含量的镉会降低钙的吸收,严重则可导致骨骼和肾脏损伤,是“痛痛病“(Itai-Itai Disease)。广泛镉中毒引起的“痛痛病”最先在日本发现[89]。也有报道称镉可能通过胰岛素下调葡萄糖转运蛋白4(GLUT4)的转运并增强诱导胰腺β细胞在糖尿病中的破坏[80]。
砷(As,砒霜):
砷是一种天然存在的致命类金属,主要用于铜合金和铅蓄电池。也常见于杀虫剂,除草剂和农药的生产中。砷是WHO列为第一类的致癌剂[80,90–92]。砷对地下水的污染正在严重威胁着全世界的人类生命[81,84,93]。砷被广泛认为是致癌物和强氧化剂,会损害神经元,肝,心血管,皮下和肾器官系统。慢性砒霜超标与糖尿病一样是全球最普遍的一大流行病(epidemic)[94]。
经常接触砷与多种疾病(包括某些类型的癌症和糖尿病)有关。研究表明,由于细细胞信号转导的改变,葡萄糖代谢被破坏,随后GLUT4易位至膜可能会被逮捕。一些研究表明砷与β细胞功能障碍有关[14,75]。
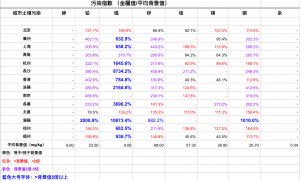
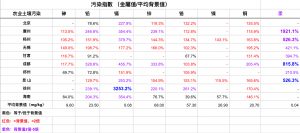
砷主要存在于地下矿物化合物中。在喜马拉雅山的岩石中尤为常见。在拥有1.67亿人口的孟加拉国,超过1亿的人患有急性砷中毒,占该东南亚国家每3个人中的2个人!由于采矿和燃煤,砷被释放到我们赖以生存的大气及地表水中,污染我们的生活环境中。大米中会积累砷,铅,汞和镉。但是砷在大米中尤其成问题,因为砷在全世界的水和土壤中都有存在,并且大米在水中的生长时间很长。大米含有维生素,矿物质和碳水化合物,但大米也有令人讨厌的地方:金属特别是无机砷(砒霜)的污染。稻米是人类饮食中无机砷污染的主要来源[93]。因此,与其他农作物相比,水稻吸收的砷是其他农作物的10-20倍。稻壳中的砷含量最高,因此糙米中的砷含量较高[93]。在过去的几十年中,中国经济的快速发展也付出了巨大的代价:环境污染,尤其是镉,砷,铅,锑[95]。
中国人中65%以大米为主食。中国人砷过量的原因中,60%被认为与大米的砷污染有关[93]。全世界一半的人口每天都吃米饭。
全美国3亿人中有约4%的人的公共饮用水中砷含量超过美国环保署(EPA)的标准(10ug/L)[96]。实际数据可能远超4%,因为有很多美国的饮水源(接近一半)没测试过的。全球而言,估计影响到4亿人口的浅层地下水有较高的无机砷[94]。海鲜,大米,蘑菇,禽类是食物中砷的主要来源。
镍(Ni)
镍是铁磁性元素,主要用于Ni-Cd电池中。大多数人口通过不同的方式暴露于镍,例如饮用污水,空气和食用受镍污染的食物[97]。已经观察到肾脏是镍积累的主要器官,因此是肾功能不全的原因[98]。Forte等人发现2型糖尿病患者血液中的镍含量较正常对照组明显升高[60]。
简而言之,研究人员分析了各种生物流体,例如血清/血浆,头发,尿液等,以便了解包括糖尿病在内的各种疾病中金属代谢的改变。在这些生物样品中,尿液是唯一的,因为它易于获取且无创采样。在一些以前发表的研究中,研究人员显示了尿液中的金属含量与他们的血清中金属含量相对应[1,14]。前述研究表明,有毒金属和必需微量金属之间存在联系[78]。